Модульный урок по теме «Сера. Оксиды серы» 10 класс
Бондаренко И.И. 4 курс,
специальность химия (образовательная),

Модульное обучение — одна из молодых альтернативных технологий и в последнее время получает широкомасштабное использование. Свое название модульное обучение получило от термина «модуль», одно из значений которого — «функциональный узел». Под модульной технологией обучения следует понимать реализацию процесса обучения путем разделения его на системы «функциональных узлов» — профессионально значимых действий и операций, которые выполняются обучаемым более или менее однозначно, что позволяет достигать запланированных результатов обучения. Сущность модульного обучения состоит в том, что оно позволяет каждому учащемуся полностью самостоятельно добиваться конкретных целей
Модуль может представлять и собой программу обучения, которая индивидуализируется по содержанию, методам обучения, уровню самостоятельности, а также темпу обучения. Модульное обучение — технология, которая позволяет перейти на субъектную основу обучения и обеспечивает ученику развитие его мотивационной сферы, интеллекта, самостоятельности, коллективизма, склонностей, умений осуществлять самоуправление
Тема: подгруппа кислорода
Модуль «Сера. Оксиды серы»
|
Номер учебного элемента
|
Учебный материал с указанием заданий
|
Управление обучением
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| УЭ-О | Интегрирующая цель: изучить особенности строения серы, химические свойства серы как окислителя и восстановителя, строение и свойства оксидов серы | Записать тему в тетрадь | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| УЭ-1 Выполнение тестовых заданий |
Цель: определить исходный уровень знаний о строении атома серы, валентности и степени окисления, нахождение в природе. Выполни тестовые задания, пользуясь периодической системой хим. элементов Задание 1 1. Сера в периодической системе хим. элементов
2. Строение внешнего электронного слоя атома серы
3. Максимальная валентность серы в соединениях равна 1. двум 2. пяти 3. четырем 4. шести 4. Сера в соединениях проявляет степень окисления
5. Сера является 1. металлом 2. неметаллом 3. переходным элементом 6. Сера в свободном состоянии является типичным 1. окислителем 2. восстановителем 7. В природе сера встречается в форме 1. сульфатов 2. сульфидов 3. сульфитов 4. всех перечисленных 8. Установите соответствие: Оксиды название степень окисления серы
|
Работай самостоятельно. В тетради запиши номер вопроса, поставь номер ответа. Задание оценивается в 8баллов. За каждый правильный ответ 1балл. Запомни правильные ответы на тестовые задания, с которыми ты не справился. При выполнении домашнего задания повтори этот материал. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| УЭ-2 Изучение нового материала |
Аллотропия серы Цель: самостоятельно изучить материал об особенностях строения аллотропных модификациях серы, определить различия в их физических свойствах. Узнать интересный факт о применении серы.
При обычных условиях устойчивая сера S8 имеет структуру короны  При температуре 95◦ С ромбическая сера переходит в моноклинную. При температуре 119◦ С она плавится около 160◦С кольца молекулы S8 разрывается, образуя бесконечные спирали. Моноклинная переходит в Интересный факт. В романе А. Дюма «Граф |
Работай самостоятельно, кратко запиши в тетрадь информацию, которая тебя удивила. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Задание 2 Укажите направление стрелок в ниже предложенной схеме «Аллотропные модификации серы», указывая условия. 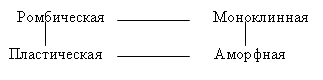 |
Перечертите схему в тетрадь. За каждое правильное направление стрелок 0,5 баллов. Всего 2 балла | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Задание 3 Заполните таблицу «Применение серы»
Сделай презентацию своей таблицы в группе, которая выставит тебе баллы. |
Выполнить в тетради. Всего 4 балла. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| УЭ-3 Изучение нового материала |
Химические свойства серы Цель: изучит особенности химических свойств серы как окислителя и восстановителя, закрепить навыки расстановки коэффициентов методом электронного баланса. 1. По материалу § подготовь, предварительно согласовав с соседом, выступление по одной из тем:
Задание 4 Впишите в пробелы отсутствующие формулы веществ с необходимыми индексами и коэффициентами. По какому признаку можно разделить эти реакции на 2 группы?
|
Записать в тетрадь уравнения реакций. За каждое правильное уравнение по 1 баллу. Всего 5баллов. Ответив на вопрос получишь 1,5 балла. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| УЭ-4 Изучение нового материала |
Оксиды серы Цель: самостоятельно изучить особенности строения оксидов серы, определить различие в их физических и химических свойствах. Изучение материала § Задание 5 Заполни сравнительную таблицу
|
Взаимооценивание в группе. За каждый правильный ответ в колонке 0,5 баллов. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| УЭ-5 Обобщении е нового материала |
Цель: обобщение и систематизация знания о сере и ее оксидах. Задание 6
|
Взаимооценивание. Каждое правильное предложение 0,5 баллов. Всего 2,5 баллов. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Задание 7 Собери схему «нахождение серы в природе» из разбросанных кубиков.  |
Задание оценивается в 2,5 балла | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Задание 8 Напишите уравнение реакции соответствующих схеме, расставьте коэффициенты.
|
За правильную запись одного уравнения 0,5 баллов. Всего 4 балла | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Подведение итогов |
Цель: определить уровень усвоения знаний по теме: «Сера и оксиды серы». Лист контроля
|
Критерии оценки 25–30 баллов оценка 5. 19–11 баллов оценка 3 Меньше 11 баллов оценка 2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
- 20297 просмотров
.webp)

.webp)